¿QUE ES LA TABLA PERIÓDICA DE LOS ELEMENTOS?
La
tabla periódica de los elementos es una disposición de los elementos químicos
en
forma
de
tabla, ordenados por su número atómico, por su configuración de electrones y
sus
propiedades
químicas. Este ordenamiento muestra tendencias periódicas, como elementos
con
comportamiento similar en la misma columna
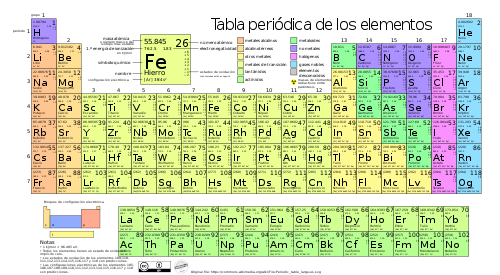 |
| TABLA PERIÓDICA DEL AÑO 2016. |
"ESTRUCTURA Y ORGANIZACIÓN DE LA TABLA PERIÓDICA".
Períodos:
Las filas horizontales de la tabla periódica son llamadas períodos. El número de niveles energéticos de un átomo determina el periodo al que pertenece.
Grupos:
A las columnas verticales de la tabla periódica se las conoce como grupos o familias. Hay 18 grupos en la tabla periódica estándar.
Bloques:
La tabla periódica se puede también dividir en bloques de acuerdo a la secuencia en la que se llenan las capas de electrones de los elementos. Cada bloque se denomina según el orbital en el que en teoría reside el último electrón
Metales, metaloides y no metales:
los elementos se pueden clasificar en tres grandes categorías: metales, metaloides y no metales. Los metales son sólidos generalmente brillantes, altamente conductores que forman aleaciones de unos con otros y compuestos iónicos similares a sales con compuestos no metálicos —siempre que no sean los gases nobles—.
¿QUIEN PRESENTO LA PRIMERA TABLA PERIÓDICA?
En este día en 1869 el químico ruso, Dimitri Mendeleev presentó la primera tabla periódica a la Sociedad Química Rusa.
Fue la culminación de un siglo de estudio de las propiedades químicas. La tabla periódica en sí misma es una representación visual de la ley periódica, que establece que cuando los elementos son ordenados de acuerdo a su peso o número atómico, ciertas propiedades de los elementos se repiten periódicamente.
Mendeleev fue recomendado para recibir el premio Nobel de Química en 1906 pero fue pasado por alto. Luego de su muerte, se nombró el elemento radiactivo número 101, mendelevium, en homenaje a él.
|
 |
Químico ruso Dimitri Mendeleev.
En primer lugar, es importante que reconozcas la forma y distribución de la tabla. La siguiente puedes imprimirla para tenerla a mano cuando la necesites o pulsar sobre ella para verla ampliada con todo detalle.
De todos modos, más adelante verás otras tablas interactivas para buscar la información que te interese en un momento dado.
Características de la tabla
• Las columnas se llaman grupos. La tabla actual consta de 18 grupos. Reciben este nombre por agrupar elementos de propiedades químicas similares.
• Las filas de la tabla se llaman periodos. Hay 7 periodos. Dentro de cada uno de ellos, los elementos están ordenados por número atómico creciente de izquierda a derecha.
• Hay dos filas de 14 elementos fuera de la tabla. En realidad, deberían estar situadas a la derecha del bario y el radio, pero se colocan fuera porque la tabla quedaría demasiado alargada, y su manejo resultaría incómodo.
Grupos cuyo nombre debes saber
1. Alcalinos.
2. Alcalinotérreos.
17. Halógenos.
18. Gases nobles.
"Historia de la tabla periódica".
En 1786, el químico francés Lavoisier intentó organizar los 30 elementos conocidos, clasificándolos como elementos metálicos, no metálicos, gases y térreos de acuerdo a sus propiedades.
En 1829, el químico alemán Döbereiner constató que ciertos grupos de tres elementos (tríadas) poseían propiedades semejantes.
En 1864, el químico inglés Newlands comparó los elementos con las notas musicales. Newlands observó que las propiedades de los elementos parecían repetirse cada 8 elementos cuando se les organizaba en orden decreciente de masa atómica. Esta ley se conoció como ley de las octavas.
Julius Lothar Meyer (químico alemán, 1830-1895) y Dimitri Mendeleyev (químico ruso, 1834-1907) desarrollaron cada uno sus propias versiones de la tabla periódica. Ambos reconocieron un patrón repetitivo en los elementos químicos conocidos hasta la primera mitad del siglo XIX.
Meyer publicó su tabla de 28 elementos por primera vez en 1864, basándose en la masa atómica y las propiedades químicas de los elementos. Mendeleyev arregló los elementos según la masa atómica y dejó espacios en blanco, prediciendo la existencia de elementos que aún no se habían descubierto. Esto le hizo ganar el reconocimiento como padre de la tabla periódica.
En 1913, Henry Moseley (1887-1915) estableció el concepto de número atómico como el aspecto clave en la organización en la tabla periódica moderna. El número atómico es el número de protones en el núcleo.
En 1945, Glenn Seaborg (1912-1997) sugirió que los elementos a partir del actinio (número 89) debían ser considerados en las tierras raras. Seaborg también contribuyó a la creación de las series de los lantánidos y actínidos, que son los periodos representados debajo de la tabla periódica.
Por: Jacob Lima Ríos
Luis Alfredo Gayosso Mota
MATERIA: QUÍMICA.
BLOQUE 4: TABLA PERIÓDICA.
|
|


Comentarios
Publicar un comentario